在适用人群分析中发现胃癌CLDN18.2表达率在42%~86% [1-6],与另外两个胃癌的靶标分子HER-2(7-30%)和PD-L1 (14-34%)的表达率相比[7-11],能从CLDN18.2获益的患者更多。
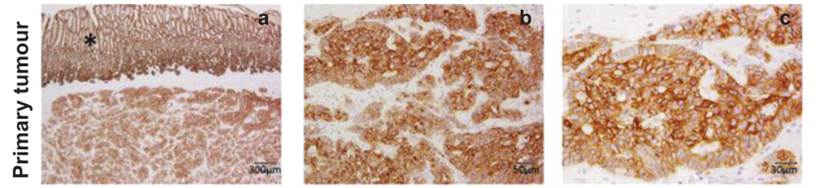
CLDN18.2在原发胃癌中的表达[12]
Zolbetuximab(IMAB362,claudixmab)是由德国生物技术公司Ganymed研发的,Ganymed是一家小型制药公司,是由如今声名鹊起的Türeci与她丈夫Uğur Şahin于2008年共同创立。Türeci就是因为新冠mRNA疫苗而一鸣惊人的BioNtech公司的首席医学家(这是后话)。IMAB362是首个靶向CLDN18.2的抗体药物,具有靶向CLDN18.2特异性,与CLDN18.1无交叉反应。在肿瘤细胞表面与CLDN18.2特异结合,从而引发抗体依赖性细胞毒性(ADCC)、补体依赖性细胞毒性(CDC),凋亡和抑制细胞增殖[13]。临床前研究已经成功地证明了它具有较强的抗肿瘤能力。随后,通过多个I/II期试验评估了其临床疗效和安全性。

Türeci与丈夫Uğur Şahin
2008年,Türeci发现CLDN18.2在正常组织中限制性表达,而在多种实体瘤中异位激活且显著性表达。此研究带给了Türeci很大的惊喜,她觉得CLDN18.2或许能够成为一种新的、极具吸引力的泛癌靶点,可用于上皮性肿瘤的抗体治疗[3]。这也是第一次表明CLDN18.2作为治疗性抗体靶标的可能性。
首战告捷
在2014年,Türeci将CLDN18.2的新抗体IMAB362应用到胰腺导管腺癌(PDAC)的研究中,发现CLDN18.2在胰腺肿瘤中的阳性率很高,大部分胰腺癌患者是有资格接受CLDN18.2靶向治疗[5]。
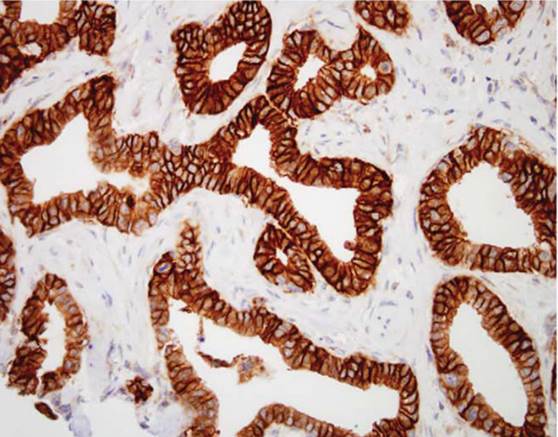
胰腺癌CLDN18免疫荧光染色更为显著[14]
声东击西
当胰腺临床研究正如火如荼时, Türeci突然将矛头转向了胃癌,并开展了多个I/II期试验,将IMAB362用于治疗晚期胃癌患者。发现IMAB362通过引发抗体依赖性细胞毒性(ADCC)、补体依赖性细胞毒性(CDC)等通路诱导胃癌细胞凋亡和抑制胃癌细胞增殖[15]。之后的临床研究进一步证实了IMAB362在CLDN18.2阳性肿瘤患者中的安全性及有效性。
暗度陈仓
2016年,日本Astellas公司以14亿美元收购Ganymed公司,其实就是为了CLDN18.2和CLDN6两支抗体。收购后将IMAB362抗体命名为zolbetuximab,之后便开展全球临床试验。而卖了公司的Türeci,转身便投入BioNTech公司(该公司成立于2008年),用于mRNA肿瘤疫苗研究。大家这才知道mRNA疫苗研究才是Türeci和Uğur Şahin夫妻俩的初心和最终梦想。
无心插柳
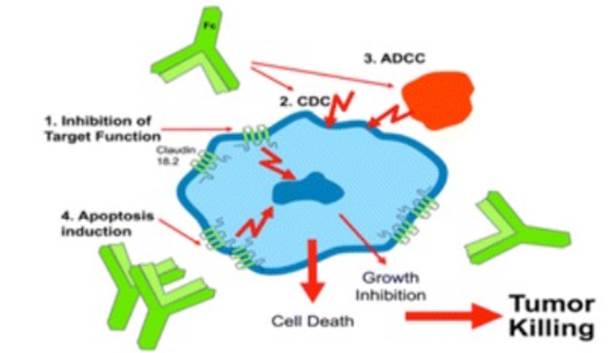
Zolbetuximab作用机制[16]
回到咱们的故事主线CLDN18.2,当前,Zolbetuximab的临床研究主要集中于晚期胃癌及胃食管交界癌患者。为了确定Zolbetuximab在人体内的最大耐受剂量,第一项人体内临床实验(NCT00909025)招募了15名CLDN18.2阳性转移性、复发性胃食管腺癌患者,该研究包含五个剂量递增队列(33、100、300、600和1000 mg/m2),结果表明Zolbetuximab在所有剂量下的耐受性良好,其中胃肠道毒性是最常见的治疗相关不良事件(TRAEs),Ⅱ期研究推荐使用600mg/m2剂量[13]。
Zolbetuximab在允许使用最佳剂量以及确保安全的情况下,同时降低了毒性,达到最大的抗癌效果。之后研究者在Ⅰ期研究的基础上又进行了一项IIa期研究(NCT01197885,MONO-2013),旨在确定Zolbetuximab单药对转移性或复发性CLDN18.2阳性胃食管腺癌患者的有效性和安全性,CLDN18.2阳性是指在>50%的肿瘤细胞中CLDN18.2染色强度≥2+,54例晚期胃食管腺癌患者每两周给药一次,对于疾病得到控制的患者继续治疗直至肿瘤进展。结果发现所有剂量药物的耐受性良好,即使在高达1000mg/m2的单剂量下仍未观察到毒性[16]。治疗效果方面4名(9%)患者部分缓解,6名(14%)患者疾病稳定,临床受益率23%,PFS提高到14.5 周[17]。
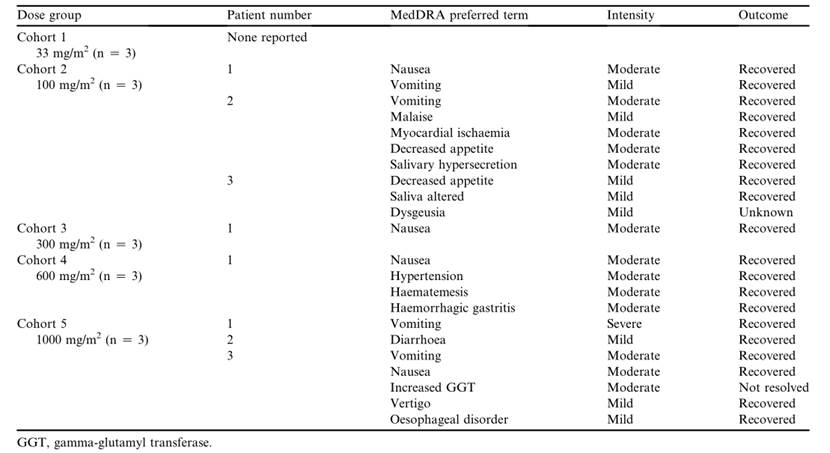
Zolbetuximab治疗相关的不良事件[13]
在2016年国际临床肿瘤学年会(ASCO)上,Ganymed公布了一项Zolbetuximab与一线(EOX)化疗联合治疗CLDN18.2阳性晚期或复发性胃食管腺癌患者疗效的临床试验结果,这一项IIb期研究(NCT01630083,FAST 2015)[18]共纳入161例患者,结果发现Zolbetuximab+EOX组中位无进展生存期(mPFS)相比EOX联合化疗组由4.8个月提高至7.9个月,总生存期由8.4个月提高至13.2个月,以及更好的客观缓解率(ORR,43% vs 28%)。另一方面,研究发现在CLDN18.2高表达(70%的肿瘤细胞CLDN18.2表达强度≥2+)的患者对Zolbetuximab有着更加显著的反应,肿瘤体积的缩小程度以及更优的疾病控制率。[19]。胃癌患者的总生存期和无进展生存期的大幅度延长使zolbetuximab成为了当年ASCO会议的最大亮点。该临床研究中看到zolbetuximab在CLDN18.2≥70%的肿瘤细胞中中度到强表达的患者存在临床效益。Zolbetuximab联合一线化疗的随机II期试验显示,CLDN18.2高表达患者的疗效更为显著。
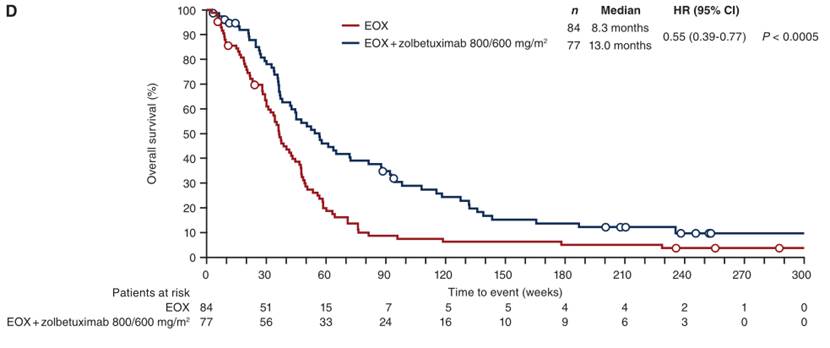
Zolbetuximab+EOX组 VS EOX组总生存期[19]
最近,Zolbetuximab正在全球范围进行两项多中心、双盲、随机Ⅲ期临床试验:NCT03653507比较Zolbetuximab+CAPOX(奥沙利铂+卡培他滨)与安慰剂+CAPOX的疗效;Zolbetuximab+mFOLFOX6(奥沙利铂+亚叶酸+氟尿嘧啶)与安慰剂+mFOLFOX6的安全性和耐受性进行评估。这两项研究都招募了CLDN18阳性、HER2阴性、局部晚期、转移性胃食管腺癌患者进行一线治疗研究。就最近Astellas公司在2022年11月公布的新闻——Ⅲ期临床研究达到PFS的主要终点,相信在不久的将来Zolbetuximab将会成为claudin 18.2靶向胃腺癌的标准治疗方法。但是值得注意的是, 似乎富集高表达CLDN18.2的患者是需要的。
CLDN18.2伴随诊断研究
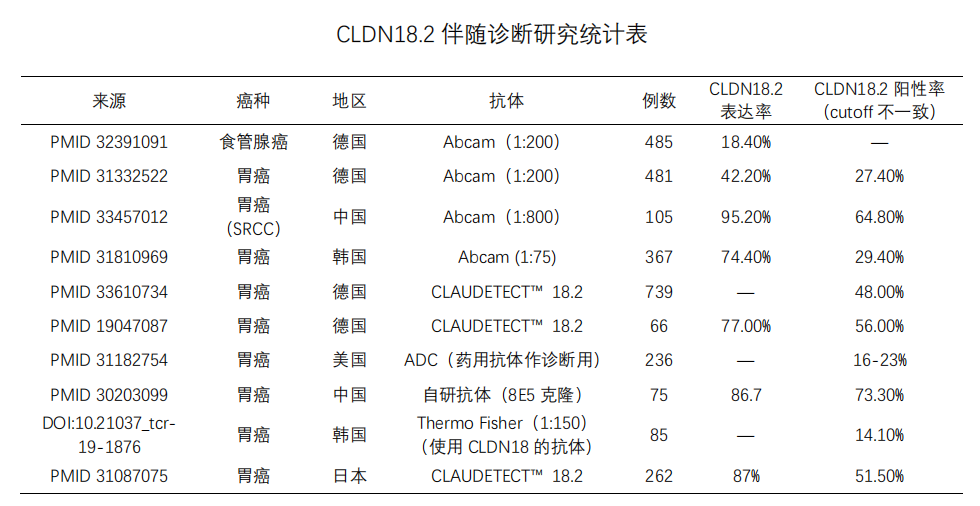
通过汇总CLDN18.2伴随诊断数据,发现虽然目前CLDN18.2的检测抗体众多,但是多数抗体不受认可。目前仅Abcam和Ganymed自己开发的检测试剂盒使用较多。有些研究人员提到,前者其特异性有待提高,后者仅提供给Ganymed公司及其合作者使用,其特异性数据未知。根据我们目前获取的数据,发现这些商品化检测抗体,基本只能用在免疫组织化学IHC。
由中科纳泰开发的CTC CLDN18.2伴随诊断技术,最早于2021年发表于《Analytical Chemistry》[20],该方法以CLDN18.2 RNA作为检测目标,开发分子探针,并建立了一套分子水平和细胞水平检测方法。
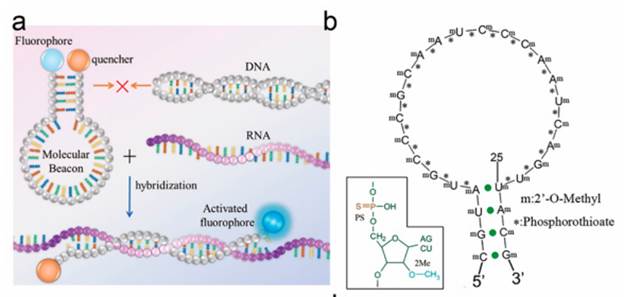
在北京大学肿瘤医院沈琳院长和张小田副院长领导下的药物临床试验中,共入组15名患者。该方法对CTC CLDN18.2 RNA表达进行三分类。发现患者CTC中CLDN18.2表达呈现较大的异质性,如果按照“+”即为阳性的标准来看,9名(60%)的CLDN18.2+ratio>50%,该结果符合临床预期。
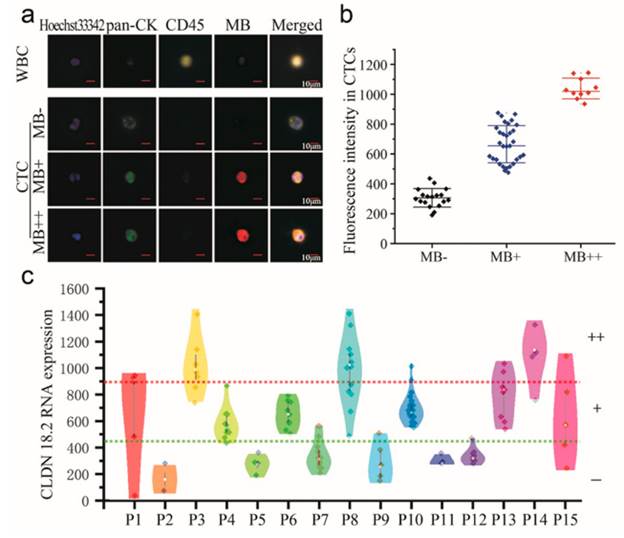
为了进一步测试CTC结果的准确性,研究获取了10名患者的IHC结果,发现除P12患者外,其他患者的IHC CLDN18.2结果与CTC结果相一致。
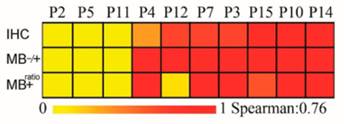
之后中科纳泰持续发力,不断优化分子探针的结构和识别区域。最终发现特异性更好的分子探针。该项目已经进行到临床测试阶段。
公司在CLDN18.2蛋白水平检测方面也开始布局,历时2年时间,筛选了众多CLDN18.2抗体,最终成功找到一支能够用于CTC检测的抗体。
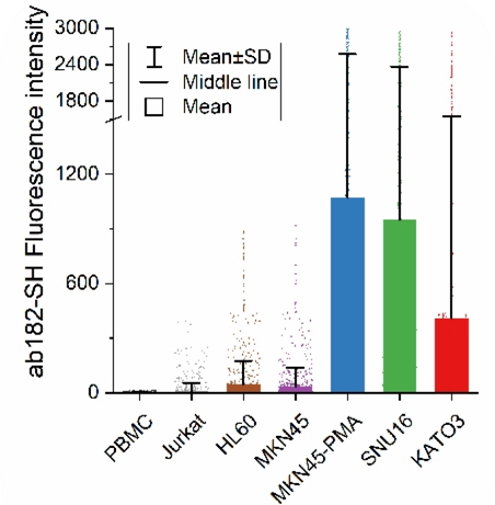
各胃癌细胞系和对照细胞检测结果统计
(PBMC,Jurkat,HL60,MKN45为CLDN18.2阴性表达细胞,MKN45-PMA,SNU16,KATO3为CLDN18.2阳性表达细胞)
总 结
参考文献
[1] Baek J H, Park D J, Kim G Y, et al. Clinical Implications of Claudin18.2 Expression in Patients With Gastric Cancer[J]. Anticancer Res, 2019, 39(12): 6973-6979.
[2] Dottermusch M, Kruger S, Behrens H M, et al. Expression of the potential therapeutic target claudin-18.2 is frequently decreased in gastric cancer: results from a large Caucasian cohort study[J]. Virchows Arch, 2019, 475(5): 563-571.
[3] Sahin U, Koslowski M, Dhaene K, et al. Claudin-18 splice variant 2 is a pan-cancer target suitable for therapeutic antibody development[J]. Clin Cancer Res, 2008, 14(23): 7624-34.
[4] Zhu G, Foletti D, Liu X, et al. Targeting CLDN18.2 by CD3 Bispecific and ADC Modalities for the Treatments of Gastric and Pancreatic Cancer[J]. Sci Rep, 2019, 9(1): 8420.
[5] Woll S, Schlitter A M, Dhaene K, et al. Claudin 18.2 is a target for IMAB362 antibody in pancreatic neoplasms[J]. Int J Cancer, 2014, 134(3): 731-9.
[6] Jiang H, Shi Z, Wang P, et al. Claudin18.2-Specific Chimeric Antigen Receptor Engineered T Cells for the Treatment of Gastric Cancer[J]. J Natl Cancer Inst, 2019, 111(4): 409-418.
[7] Böger C, Behrens H M, Mathiak M, et al. PD-L1 is an independent prognostic predictor in gastric cancer of Western patients[J]. Oncotarget, 2016, 7(17): 24269-83.
[8] Kawazoe A, Kuwata T, Kuboki Y, et al. Clinicopathological features of programmed death ligand 1 expression with tumor-infiltrating lymphocyte, mismatch repair, and Epstein-Barr virus status in a large cohort of gastric cancer patients[J]. Gastric Cancer, 2017, 20(3): 407-415.
[9] Li Z, Lai Y, Sun L, et al. PD-L1 expression is associated with massive lymphocyte infiltration and histology in gastric cancer[J]. Hum Pathol, 2016, 55: 182-9.
[10] Saito R, Abe H, Kunita A, et al. Overexpression and gene amplification of PD-L1 in cancer cells and PD-L1(+) immune cells in Epstein-Barr virus-associated gastric cancer: the prognostic implications[J]. Mod Pathol, 2017, 30(3): 427-439.
[11] Dai C, Geng R, Wang C, et al. Concordance of immune checkpoints within tumor immune contexture and their prognostic significance in gastric cancer[J]. Mol Oncol, 2016, 10(10): 1551-1558.
[12] Rohde C, Yamaguchi R, Mukhina S, et al. Comparison of Claudin 18.2 expression in primary tumors and lymph node metastases in Japanese patients with gastric adenocarcinoma[J]. Jpn J Clin Oncol, 2019, 49(9): 870-876.
[13] Sahin U, Schuler M, Richly H, et al. A phase I dose-escalation study of IMAB362 (Zolbetuximab) in patients with advanced gastric and gastro-oesophageal junction cancer[J]. Eur J Cancer, 2018, 100: 17-26.
[14] Karanjawala Z E, Illei P B, Ashfaq R, et al. New markers of pancreatic cancer identified through differential gene expression analyses: claudin 18 and annexin A8[J]. Am J Surg Pathol, 2008, 32(2): 188-96.
[15] Tureci, Mitnacht-Kraus R, Woll S, et al. Characterization of zolbetuximab in pancreatic cancer models[J]. Oncoimmunology, 2019, 8(1): e1523096.
[16] Singh P, Toom S, Huang Y. Anti-claudin 18.2 antibody as new targeted therapy for advanced gastric cancer[J]. J Hematol Oncol, 2017, 10(1): 105.
[17] Tureci O, Sahin U, Schulze-Bergkamen H, et al. A multicentre, phase IIa study of zolbetuximab as a single agent in patients with recurrent or refractory advanced adenocarcinoma of the stomach or lower oesophagus: the MONO study[J]. Ann Oncol, 2019, 30(9): 1487-1495.
[18] Zhang J, Dong R, Shen L. Evaluation and reflection on claudin 18.2 targeting therapy in advanced gastric cancer[J]. Chin J Cancer Res, 2020, 32(2): 263-270.
[19] Sahin U, Tureci O, Manikhas G, et al. FAST: a randomised phase II study of zolbetuximab (IMAB362) plus EOX versus EOX alone for first-line treatment of advanced CLDN18.2-positive gastric and gastro-oesophageal adenocarcinoma[J]. Ann Oncol, 2021, 32(5): 609-619.
[20] Fan L, Chong X, Zhao M, et al. Ultrasensitive Gastric Cancer Circulating Tumor Cellular CLDN18.2 RNA Detection Based on a Molecular Beacon[J]. Anal Chem, 2021, 93(2): 665-670.


